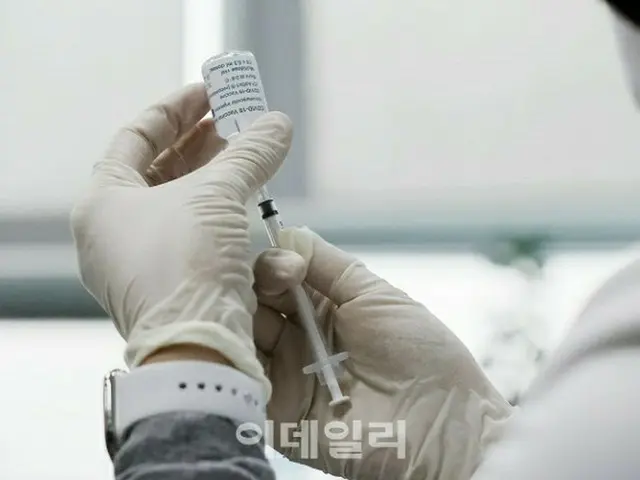
26日(現地時間)ニューヨークタイムズ(NYT)によると、FDAは ファイザー社とモデルナ社が初めに計画した5歳から11歳の幼児を対象とした臨床試験を実施するのに「その規模と範囲では、ワクチンの稀な副反応を探知するには足りない」という見解を伝えた。
FDAは これらの製薬企業に、幼児を対象とした臨床試験において 心臓に関連した稀な副反応を よりきちんと探知するために、試験の参加者を本来の計画であった人数の2倍に達する3000人へと増やすことを注文した。
「今回の臨床試験の拡大方針が、ジョー・バイデン米大統領が先週 言及した “幼児に対するワクチンの緊急使用承認の時期”に影響を与えるかについては不透明だ」と、NYTは伝えた。
Copyrights(C) Edaily wowkorea.jp 96